A 19. század végén, Dmitrij Mendelejev orosz kémikus megjelent első kísérlete a vegyi elemek csoportosítása az atomtömegük szerint. Mindössze 60 elem volt ismert abban az időben, de Mendelejev rájött, hogy amikor az elemek súly szerint vannak rendezve, bizonyos típusú elemek rendszeres időközönként vagy időszakonként fordulnak elő.
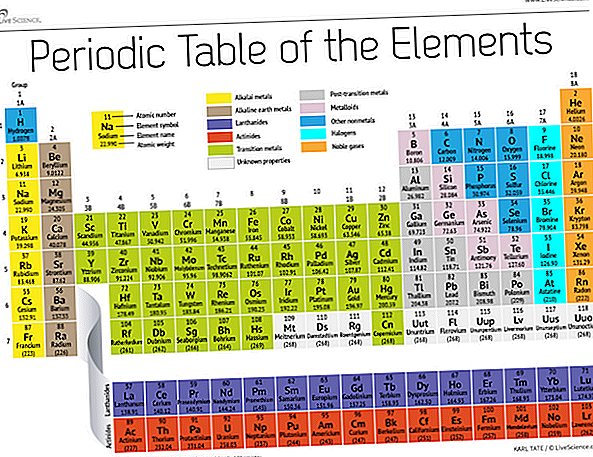
Ma, 150 évvel később, a vegyészek hivatalosan elismernek 118 elemet (miután négy újonnan csatlakoztak 2016-ban), és továbbra is a Mendelejev periodikus elemtábláját használják ezek szervezéséhez. A táblázat a legegyszerűbb atommal, a hidrogénnel kezdődik, majd a többi elemet atomszám szerint rendezi, azaz az egyes protonok számát. Néhány kivétellel az elemek sorrendje megegyezik az egyes atomok növekvő tömegével.
A táblázat hét sorból és 18 oszlopból áll. Minden sor egy periódust ábrázol; az elem periódusa azt jelzi, hogy az energiaszintje hány ház elektronot tartalmaz. Például a nátrium a harmadik időszakban ül, ami azt jelenti, hogy a nátrium-atom elektronjai általában az első három energiaszinten vannak. Az asztal lefelé haladva az időszakok hosszabbak, mert több elektronra van szükség a nagyobb és összetettebb külső szintek kitöltéséhez.
A táblázat oszlopai az elemek csoportjait vagy családjait ábrázolják. A csoport elemei gyakran hasonlóan néznek ki és viselkednek, mert ugyanolyan számú elektron van a legkülső héjukban - az arcuk, amelyet a világnak mutatnak. A 18. csoport elemei, például az asztal jobb szélén, teljesen teljes héjjal rendelkeznek, és ritkán vesznek részt a kémiai reakciókban.
Az elemeket általában fém vagy nem fémből osztályozzák, de a kettő közötti elválasztó vonal homályos. A fém elemek általában jó villamos és hővezetők. A fémek alcsoportjai ezen gyűjtemények hasonló tulajdonságain és kémiai tulajdonságain alapulnak. A periódusos táblázat leírása az általánosan elfogadott elemcsoportokat használja, a Los Alamos Nemzeti Laboratórium szerint.
Alkálifémek: Az alkálifémek képezik az 1. csoport nagy részét, a táblázat első oszlopát. Ezek a fémek, amelyek fényesek és elég puhaak, hogy késbe vágják, lítiummal (Li) kezdődnek, és franciával (Fr) végződnek. Rendkívül reakcióképesek és lángba robbannak, vagy vízzel érintkezve felrobbannak, így a vegyészek olajokban vagy inert gázokban tárolják őket. A hidrogén, egyetlen elektronjával, szintén az 1. csoportban él, de a gázt nemfémesnek tekintik.
Alkáliföldfémek: Az alkáliföldfémek képezik a periódusos táblázat 2. csoportját, a berilliumból (Be) a rádiumig (Ra). Ezen elemek mindegyikének két elektronja van a legkülső energiaszintjén, ami elegendő reakcióképessé teszi az alkáliföldféket, hogy ritkán forduljanak elő egyedül a természetben. De nem olyan reakcióképes, mint az alkálifémek. Kémiai reakcióik általában lassabban zajlanak le és kevesebb hőt termelnek az alkálifémekhez képest.
Lantanidák: A harmadik csoport túlságosan hosszú ahhoz, hogy beleférjen a harmadik oszlopba, tehát kitört és oldalra esik, hogy az asztal alján lebegő sziget felső sorává váljanak. Ez a lantanidok, az 57–71. Elemek - lantán (La) - lutecium (Lu). Az ebbe a csoportba tartozó elemek ezüstös fehér színűek, és a levegővel érintkezve elhalványulnak.
aktinidek: Az aktinidák a sziget alsó sorát vonják magukba, és 89 elemeket tartalmaznak, aktiniumot (Ac), átmenőleg 103-ig, lawrenciumot (Lr). Ezen elemek közül csak a tórium (Th) és az urán (U) fordul elő természetesen a Földön jelentős mennyiségben. Valamennyi radioaktív. Az aktinidek és a lantanidok együttesen egy belső átmeneti fémeknek nevezett csoportot alkotnak.
Átmeneti fémek: Visszatérve az asztal fő részéhez, a 3–12. Csoport többi része az átmeneti fémek többi részét képviseli. Kemény, de alakítható, fényes és jó vezetőképességgel rendelkezik, ezekre az elemekre gondolsz általában, amikor meghallja a fém szót. A fémvilág legnagyobb slágerei - beleértve az aranyat, az ezüstöt, a vasat és a platinát - itt élnek.
Átmeneti fémek: A nemfémes világba való ugrás előtt a közös jellemzők nem oszlanak el megfelelően a függőleges csoportvonalak mentén. Az átmenetek utáni fémek: alumínium (Al), gallium (Ga), indium (In), tallium (Tl), ón (Sn), ólom (Pb) és bizmut (Bi), és a 13. csoportot a 17. csoportba foglalják. Ezeknek az elemeknek vannak az átmeneti fémek klasszikus tulajdonságai, ám ezek lágyabbak és gyengébben vezetnek, mint más átmeneti fémek. Számos periódusos rendszerben egy csavart "lépcső" vonal szerepel az átló alatt, amely összeköti a bórot az asztatinnal. Az átmenet utáni fémek csoportosulnak ennek a sornak a bal alsó részén.
Nemfémes: A metalloidok bór (B), szilícium (Si), germánium (Ge), arzén (As), antimon (Sb), tellúr (Te) és polónium (Po). Ezek a lépcsők képezik a fémekről a nem fémekre történő fokozatos átmenetet. Ezek az elemek időnként félvezetőkként viselkednek (B, Si, Ge), és nem vezetőkként. A metalloidokat "fémből" vagy "gyenge fémeknek" is nevezik.
nemfémek: Minden, ami a lépcső jobb felső sarkában van, plusz hidrogén (H), az 1-es csoportba visszatekintve, nem metál. Ide tartoznak a szén (C), a nitrogén (N), a foszfor (P), az oxigén (O), a kén (S) és a szelén (Se).
A halogének: A 17. csoport négy legfontosabb eleme, a fluorból (F) az asztatinnal (At) kezdve, a nemfémek két részhalmazának egyikét képviseli. A halogének meglehetősen kémiailag reagálnak és hajlamosak párosulni alkálifémekkel különféle sók előállítására. Például a konyhában lévő asztali só házasság az alkálifém-nátrium és a halogén-klór között.
Nemesgázok: Színtelen, szagtalan és szinte teljesen nem reaktív, a közömbös vagy nemes gázok a 18. csoportban a táblázatot veszik körül. Sok vegyész azt várja, hogy az oganesson, a négy újonnan megnevezett elem egyike, megosszák ezeket a jellemzőket; Mivel ennek az elemnek a felezési ideje milliszekundumban van, senki sem volt képes közvetlenül tesztelni. Az Oganesson befejezi a periódusos rendszer hetedik periódusát, tehát ha valakinek sikerül a 119. elemet szintetizálni (és az erre irányuló verseny már folyamatban van), akkor körbefordul, és elindul a nyolcadik sor az alkálifém oszlopban.
Mivel a ciklikus természet következtében a periodikusság teremti meg a nevét az asztalnak, egyes vegyészek inkább Mendelejev asztalát körként jelenítik meg.
További erőforrások: